MDCG Subgroups于2023年3月10日发布了指南文件工作计划,内容涉及公告机构监督(Notified Bodies Oversight, NBO)、上市后监督和警戒(Post-Market Surveillance and Vigilance, PMSV)、市场监控(Market Surveillance, MS)和医疗器械命名(Nomenclature)等多项内容。
MDCG Subgroups接下来的工作重点之一是对公告机构认证能力的提高和认证水平的规范。根据本次的工作计划,MDCG即将发布的NBO指南文件有6条,如下所示:
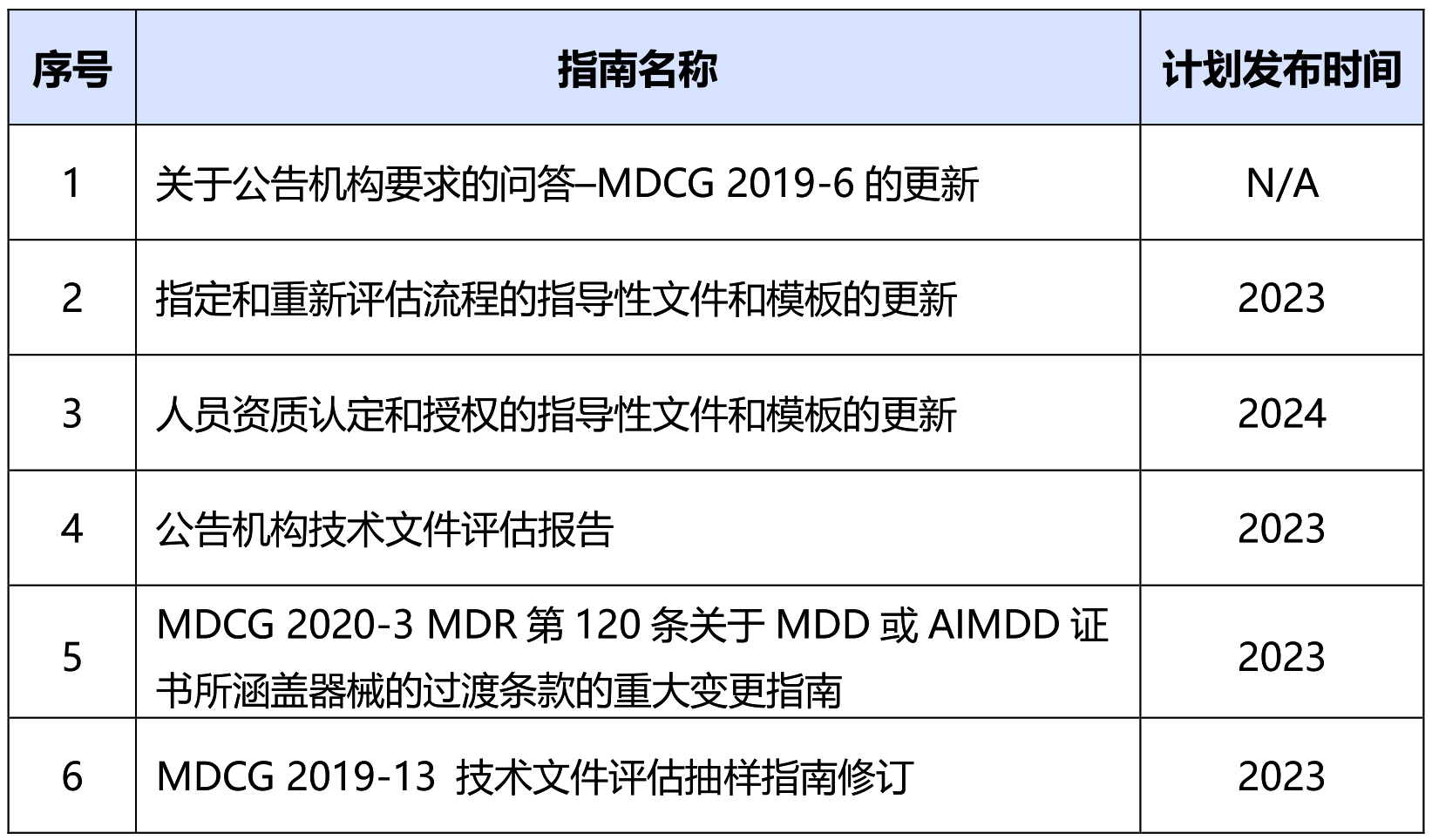
除NBO外,PMSV和MS也是本次工作计划中的侧重点,涉及的指南文件有9条。MDR附录Ⅰ强调应尽可能降低风险,降低风险不仅要求制造商通过包括设计开发在内的完善的质量体系,还需医疗器械监管体系、上市后监管、市场监控等外部保障。MDCG即将推出的PMSV和MS指南文件如下:
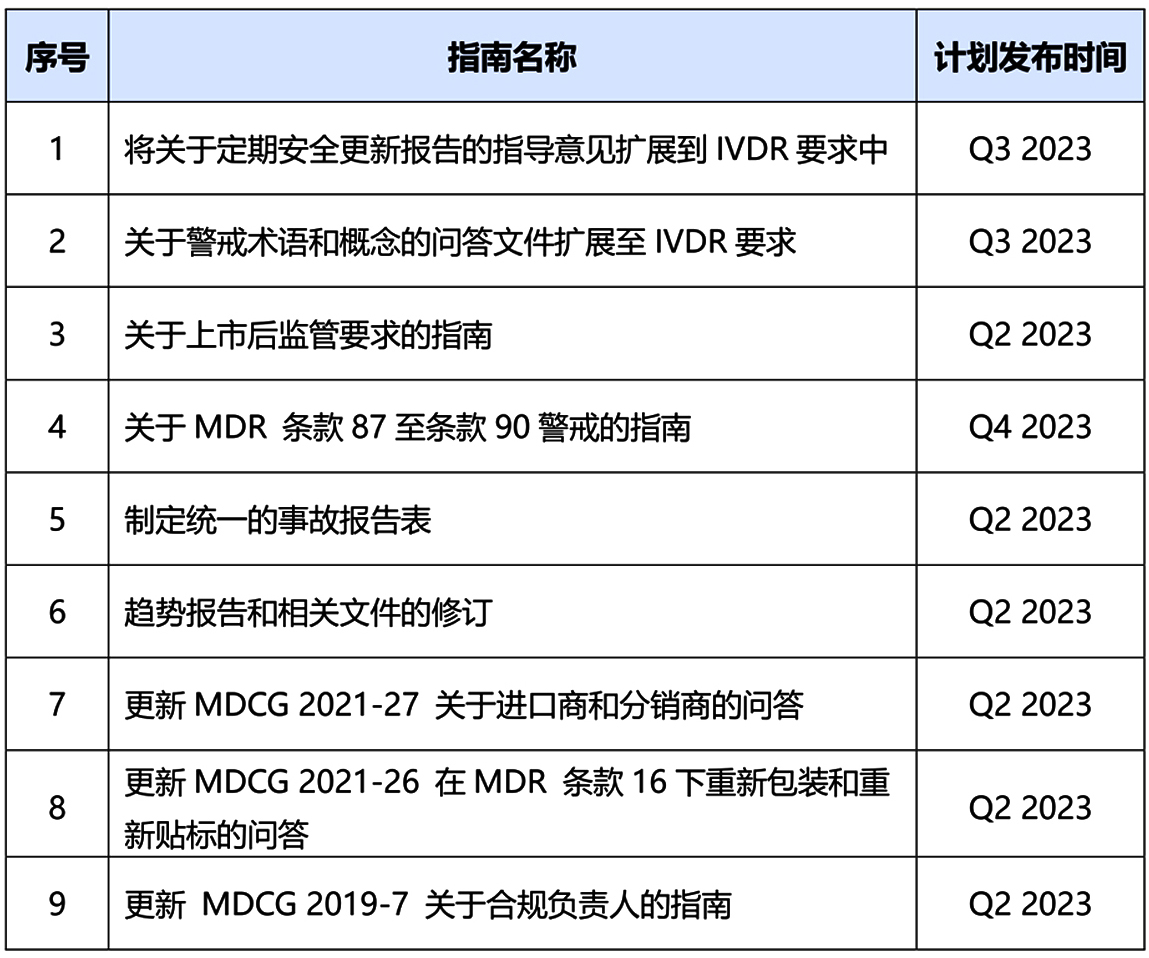
在MDCG Subgroups发布的指南发布工作计划中,小编注意到有份指南为“EMDN和GMDN的映射”。根据MDR法规第26条和IVDR法规第23条,EMDN(欧洲医疗器械命名系统)旨在支持欧洲医疗器械数据库(EUDAMED)的运作。制造商在EUDAMED中进行医疗器械注册时,应为医疗器械分配一个EMDN代码,并与每个UDI-DI相关联。GMDN(全球医疗器械术语系统)目前受国际医疗器械监管者论坛(IMDRF)推荐,被70多个国家的医疗器械监管机构用作支持其活动的术语系统,包括美国、加拿大、澳大利亚、巴西和俄罗斯等。如能实现EMDN到GMDN的映射,将方便目前使用GMDN进行其他区域注册,比如FDA UDI数据库的运营商。MDCG Subgroups对于EMDN相关指南的工作计划如下表所示:
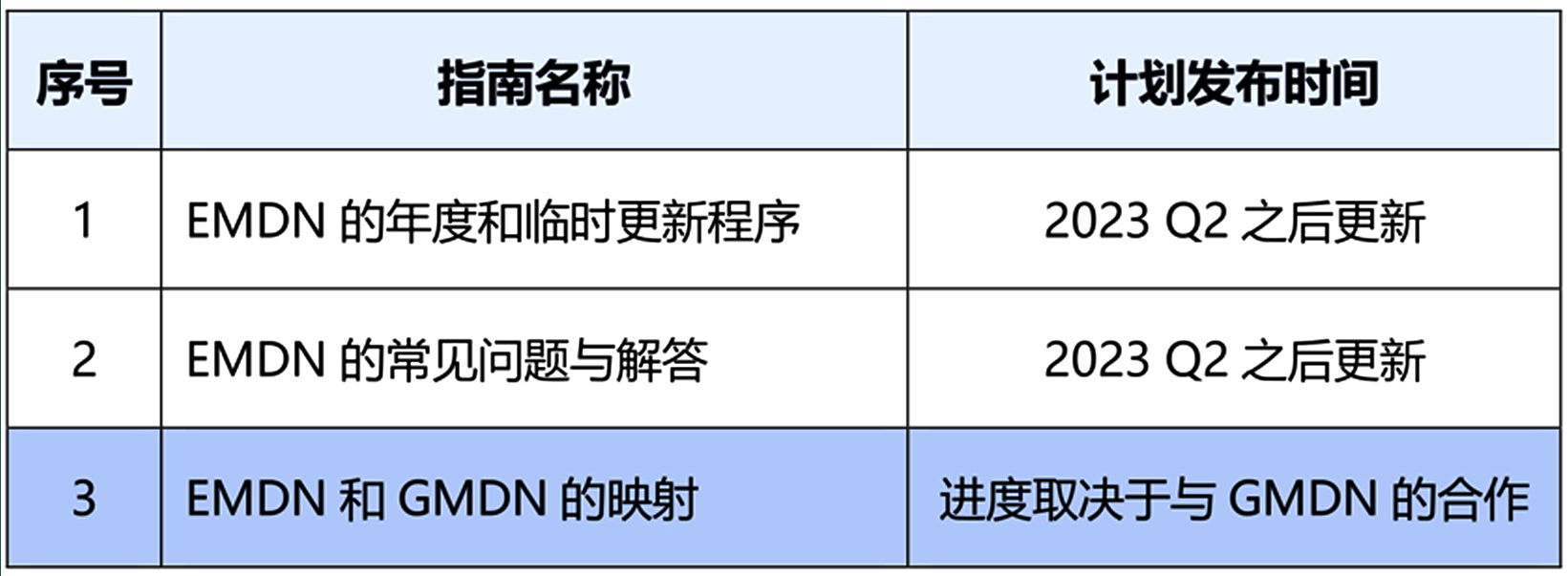
参考信息:



