摘要:自2023年10月1日起,除豁免之外,所有510(k)申请必须使用eSTAR在线递交。在进一步通知发布之前,De Novo申请可以自愿选择使用eCopy或eSTAR递交。
美国FDA于2023年3月20日升级了CDRH门户网站,并要求医疗器械商自2023年10月1日起,除豁免之外,所有510(k)申请必须使用eSTAR(electronic Submission Template And Resource)在线递交。在进一步通知发布之前,De Novo申请可以自愿选择使用eCopy或eSTAR递交。本消息要点如下表所示:
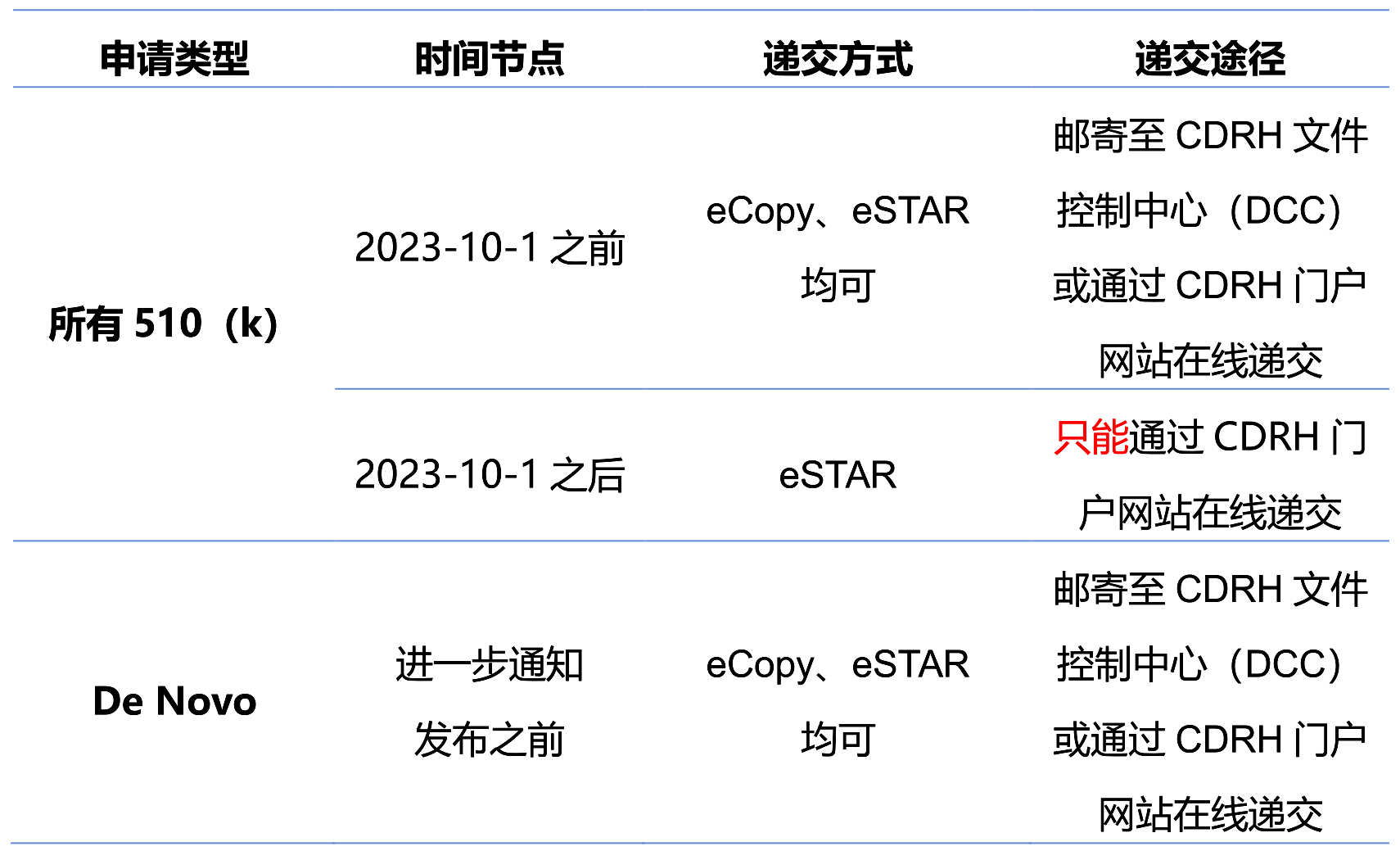
目前,eSTAR仅适用于递交给CDRH或CBER的510(k)和De Novo申请,组合产品尚不可通过eSTAR递交申请。
什么是eSTAR?
eSTAR是一种带有嵌入功能的PDF模板,用于指导申请人准备一份全面的医疗器械申请。eSTAR是目前唯一一种电子递交模板。为了简单起见,使用此电子递交模板创建的电子递交通常被称为eSTAR。eSTAR旨在提高递交一致性和审查效率。
eSTAR模板包含:自动化(如表格构建和自动填写);CDRH内部审查模板相对应的内容和结构;多种资源整合(如指南和数据库);对每个递交部分进行指导性构建;自动验证。
eSTAR递交tips
除了满足eSTAR电子递交模板架构里的信息,任何递交过程中的小细节都不容忽视:
eSTAR vs eCopy
eCopy是指递交的医疗器械申请资料的电子副本,通过CD、DVD或闪存驱动器创建,递交时附有一份签名的申请信纸质原件。需要注意的是,eCopy必须符合《eCopy Program for Medical Device Submissions》的要求,如出现文件命名规则、命名格式等不符合,则会导致审核暂停,从而影响注册进度。
eSTAR带有自动验证功能,FDA不打算对以eSTAR方式递交的申请进行RTA(Refuse to Accept)审查,因而可节省第一阶段审核及发补时间。同时,由于eSTAR拥有与CDRH内部审查模板相对应的内容和结构,并且能添加备注,从FDA对注册资料的审核角度看,eSTAR将能大大地提高审核的效率和质量。
与eCopy相比,eSTAR递交内容没有实质性变化,但对文档框架有所调整,比如,把网络安全/互操作性、分类、灭菌、协调标准、参考文献这些信息作为单独的章节来描述。
参考资料:



