【征求意见】骨科植入物注册技术导则家族增添新成员!
日期:2020年12月04日
苏州大学卫生与环境技术研究所
阅读量:3456
2020年12月01日,国家药品监督管理局医疗器械技术审评中心公示关于公开征求《可降解镁金属骨科植入物注册技术审查指导原则(征求意见稿)》意见的通知,旨在应对医疗器械领域新材料、新技术的研发,促进新材料、新技术转化。原文如下:

敲黑板,划重点!
一、适用范围
- 主要以镁金属接骨螺钉产品为例;
- 其他临床用途的镁金属骨科植入物产品、其他可降解金属材料、含有涂层的相关产品结合使用情况参考本指导原则适用部分。
二、注册单元的划分
- 申报产品主要组成部分的材质、制造工艺、适用范围、关键性能指标不同的产品应划分为不同的注册单元。
三、注册申报资料要求
1、综述资料
- 管理类别、分类编码及规范性命名:依据《医疗器械分类规则》、《医疗器械通用名称命名规则》;
- 产品描述:描述产品各组成部分材料的化学成分及比例、结构组成、与人体接触部位的界面结构和连接方式和降解机理等;
- 型号规格:描述产品各型号的关键尺寸参数(范围)和允差;
- 包装说明:利用包装结构解析图和列表形式明示信息;
- 适用范围和禁忌症:与临床评价资料结论保持一致;
- 参考的同类产品或前代产品:提供同类产品或前代产品的信息,阐述申报产品的研发背景和目的。
2、研究资料
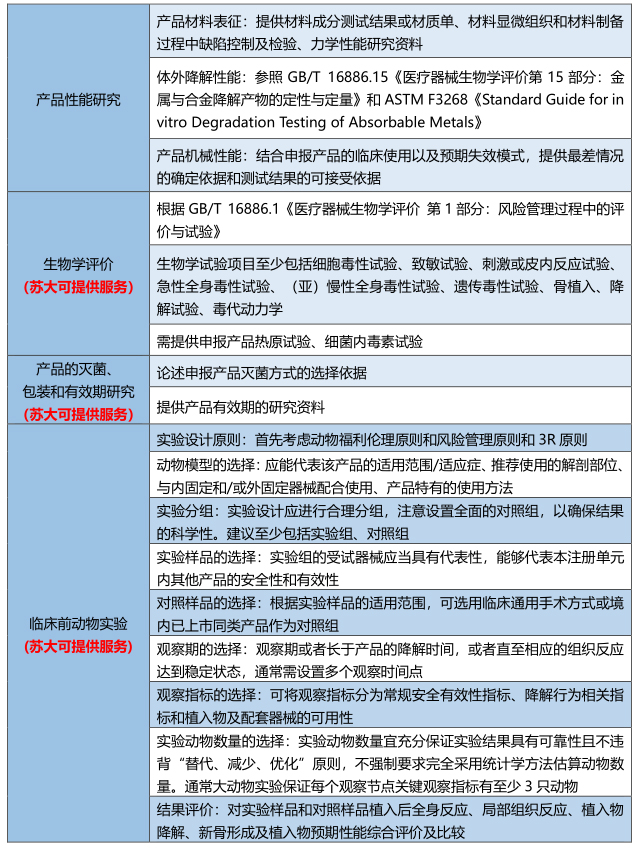
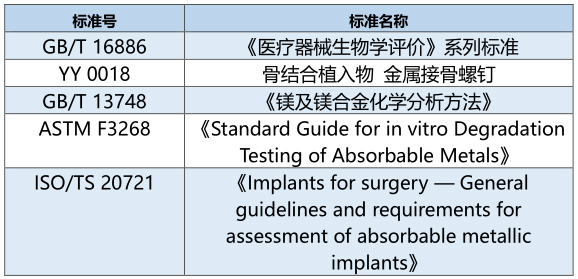
3、可参考的标准举例
四、生产制造信息
- 描述工艺原理和过程,提供切削液、清洗验证等资料,注明关键工艺和特殊过程,说明过程控制点及控制标准。
五、临床评价资料
- 在满足注册法规要求的前提下,按照《医疗器械临床评价技术指导原则》的要求选择合适的临床评价路径提交临床评价资料;
- 对于需要进行临床试验的,应严格按照《医疗器械临床试验质量管理规范》进行临床试验;
- 境外注册申请人如有境外临床试验数据,可参照《接受医疗器械境外临床试验数据技术指导原则》。
六、产品风险管理资料
- 根据YY/T 0316-2016《医疗器械风险管理对医疗器械的应用》,充分识别可降解镁金属骨植入物全生命周期各环节的安全特征;
- 提供产品上市前对其风险管理活动进行全面评审所形成的风险管理报告;
- 风险管理报告应包括风险分析、风险评价、风险控制等产品风险管理的相关资料。
七、产品技术要求
- 应按照《医疗器械产品技术要求编写指导原则》进行编写;
- 指标应针对终产品制定,且性能指标不应低于产品适用的强制性国家标准和/或强制性行业标准。
八、产品注册检验报告
- 同一注册单元内所检测的产品应当是能够代表本注册单元内其他产品安全性和有效性的典型产品;
- 应选择结构最复杂、性能指标覆盖最多的型号作为典型型号进行检验。
九、说明书和标签样稿
- 应符合《医疗器械说明书和标签管理规定》要求,还应符合相关国家标准、行业标准的要求;
- 产品说明书中适用范围、适应症、禁忌症、警告、注意事项等信息应与临床评价资料中确认的相关内容一致;
- 应在说明书予以明确是否能与其他材料配合使用并提交支持性资料。
原文链接:https://www.cmde.org.cn/CL0004/22060.html
【原文来源】国家药品监督管理局医疗器械技术审评中心
【全文整理】苏州大学卫生与环境技术研究所
【声明】如果您认为我们的内容或来源标注与原文不符,请告知我们,我们将与您积极协商解决。谢谢大家的关注。